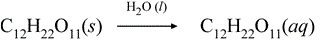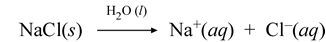Forskjellige blandinger
I
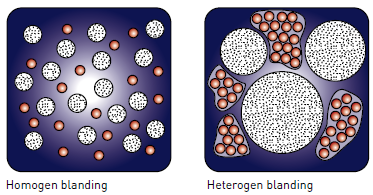
naturen finnes det sjeldent homogene (ensartet) stoffer, både i ferskvann og saltvann finnes det blanding av vann og mange andre
stoffer. En homogen blanding er en blanding av to eller flere stoffer, og blir
definert som en løsning. I en homogen blanding er et av stoffene egnet som
løsemiddel. Ordet løsning brukes ofte i forbindelse når faste stoffer eller
gasser blir løst opp i en væske f.eks. alkohol i vann. En heterogen blanding
er en blanding av ulike stoffer og kan være ujevnt fordelt, f.eks. en blanding av oljedråper i vann. Mange heterogene blandinger kan ses direkte
med øyene eller gjennom mikroskop.
I enhver løsningsprosess må både bindingene mellom molekylene eller ionene i stoffet som skal løses, og bindingene mellom molekylene i løsemiddelet bli brutt. For å danne bindinger mellom molekylene eller ionene i det løse stoffet og løsemiddelet.
Vann er polart og egner seg godt som løsemiddel for polare stoffer. Det betyr at vann fungerer dårlig som løsemiddel for upolare stoffer, som oksygengass, metan, bensin og olje. Upolare stoffer er koblet sammen med dipolbindinger (van der Waals-bindinger). Siden dipolbindinger er svakere enn hydrogenbindinger, vil de ikke er i stand til å bryte hydrogenbindingene mellom vannmolekylene. Da benyttes andre løsemidler, f.eks. white-spirit og eter som består av upolare molekyler bundet sammen av dipolbindinger. Uttrykket «lik løser lik» brukes ved at polare løsemidler løser polare stoffer, og upolare løsemidler løser upolare stoffer.
Løseligheten varier fra stoff til stoff, og er i tillegg avhengig av den rette temperaturen. Når temperaturen stiger i en beholder som inneholder en gass i en væske, vil løseligheten avta. Men for faste stoffer i en væske vil løseligheten øke. Enheten for løselighet er mol/L, også kalt M, molar. Løseligheten til salter varierer ut ifra tiltrekningskraften mellom ionene i det faste saltet. Løselighet deles inn i lettløselighet, tungtløselig og uløselig salter, og det finnes ingen skarpe grenser mellom de tre typene. Noen lettløselige salter er natriumioner, kaliumioner, ammonium og nitrat.
I enhver løsningsprosess må både bindingene mellom molekylene eller ionene i stoffet som skal løses, og bindingene mellom molekylene i løsemiddelet bli brutt. For å danne bindinger mellom molekylene eller ionene i det løse stoffet og løsemiddelet.
Vann er polart og egner seg godt som løsemiddel for polare stoffer. Det betyr at vann fungerer dårlig som løsemiddel for upolare stoffer, som oksygengass, metan, bensin og olje. Upolare stoffer er koblet sammen med dipolbindinger (van der Waals-bindinger). Siden dipolbindinger er svakere enn hydrogenbindinger, vil de ikke er i stand til å bryte hydrogenbindingene mellom vannmolekylene. Da benyttes andre løsemidler, f.eks. white-spirit og eter som består av upolare molekyler bundet sammen av dipolbindinger. Uttrykket «lik løser lik» brukes ved at polare løsemidler løser polare stoffer, og upolare løsemidler løser upolare stoffer.
Løseligheten varier fra stoff til stoff, og er i tillegg avhengig av den rette temperaturen. Når temperaturen stiger i en beholder som inneholder en gass i en væske, vil løseligheten avta. Men for faste stoffer i en væske vil løseligheten øke. Enheten for løselighet er mol/L, også kalt M, molar. Løseligheten til salter varierer ut ifra tiltrekningskraften mellom ionene i det faste saltet. Løselighet deles inn i lettløselighet, tungtløselig og uløselig salter, og det finnes ingen skarpe grenser mellom de tre typene. Noen lettløselige salter er natriumioner, kaliumioner, ammonium og nitrat.
Vann som løsemiddel

Vann er polart og egner seg godt som løsemiddel for andre polare stoffer. Når en sukkerbit puttes i vann, vil den bli oppløst. Rørsukkeret er et disakkarid, som er bygd opp av sukrosemolekyler, C12H22O11. Siden sukker løser seg opp i vann, må sukkeret inneholde noen polare molekyler. Under løsningsprosessen brytes bindinger i vannmolekyler og sukkermolekyler. De frie sukkermolekylene blir omgitt av vannmolekyler, og blir bundet sammen av hydrogenbindinger. En slik løsning kalles ikke-elektrolytt dvs. at den kan ikke lede strøm. Når det blir tilsatt mer vann vil løsningen bli tynnet ut, men hvis det blir tilsatt flere sukkerbiter, vil løsningen bli mer konsentrert. Så snart løsningen ikke kan løses mer, er løsningen mettet. Hvis løsningen er mindre konsentrert enn i en mettet løsning, er løsningen umettet. I en mettet løsning vil sukker hele tiden bli løst opp i vann, men det oppløste sukkeret vil samtidig begynne å krystallisere. I begynnelsen vil det være flere oppløste sukkermolekyler enn det krystalliseres. Etter hvert vil oppløsningshastigheten lik krystalliseringshastigheten. Det blir dannet en kjemisk likevekt, som skrives slik:
Hvis løsningen blir mer konsentrert enn en mettet løsning er løsningen overmettet. For å kunne lage en overmettet løsning må man vurdere ut ifra at den mettede løsningen har høy temperatur. For å få en overmettet løsning må man prøve å forsinke krystallisasjonen. Dette kan oppnås ved å ta bort stoffer som ikke har løst seg, avkjøler løsningen langsomt, har den i ro og hindrer at andre stoffer kommer i kontakt. Når løsningen er overmettet, blir den ustabil.
Hydratiserte ioner og krystallvann
Hydratiserte ioner er når salter løser seg i vann, for eksempel natriumklorid (NaCl) som er bygd opp av positive natriumioner og negative kloridioner i et ionegitter/krystall. Krystallen holdes sammen av ionebindinger. Når saltet blir løst i vann, vil positive natriumioner bli tiltrukket av de negative oksygensidene hos vannmolekylet. Dette fører til at natriumionene blir ført ut i væsken, det samme gjelder for kloridionene og hydrogenatomene. Løsningsreaksjonen skrives slik:
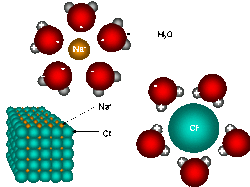
Denne løsningen blir kalt elektrolytt, fordi den inneholder mange ioner som leder elektrisk strøm. Ioner som er omringet av vannmolekyler kalles hydratiserte ioner. Det blir dannet svake ion-dipol-binding mellom vannmolekylet og ionet. Når de hydratiserte ionene krystalliseres til fast stoff, vil vannet bli utskilt, for ikke å inntre i natriumkloridgitteret. Det finnes enkelte tilfeller av salter, der vannmolekylene blir sterkt bundet til ionene, og blir dratt inn i krystallgitteret under krystallisasjonen. Vann som inntres på denne måten kalles krystallvann.
Noen eksempler på salter med krystallvann er:
- Berylliumklorid (BeCl2 *4H2O)
- Jern(II)sulfat (FeSO4 *7H2O)
- Magnesiumklorid (MgCl2 *6H20)
- Natriumsulfat (Na2SO4*10H2O)
- Aluminiumklorid (AlCl3*6H2O)
Bindingen mellom saltene og vannmolekylene er svake, dvs. når et fast stoff som inneholder vannkrystaller blir varmet opp vil vannet bli skylt ut. Krystallvann kan ha en innvirkning på egenskapene til salter, for eksempel kan jern(II)klorid (FeCl2) gå fra å være gulgrønn til å bli blågrønn når det tilsettes krystallvann. Noen salter kan ta opp vann fra lufta og danne vannkrystaller, det gjelder både for kobber(II)sulfat og kalsiumklorid. Salt med krystallvann f.eks. AlCl3*6H2O leses aluminiumkloridheksahydrat, men kan også leses «vann»: aluminiumklorid-seks-vann. Symbolet for et ion som er hydratisert skrives aq (aqua).
I fellesreaksjoner blir det dannet et bunnfall, f.eks. når natriumklorid og sølvnitrat blandes i en vannløsning, blir det dannet et hvitt, fast stoff som bunnfall. Ioner som finnes i løsningen, men som ikke deltar under reaksjonen kalles tilskuerioner, og beholder formen sin under hele reaksjonen.